The final launch of the Allmultimedia.org will take place on February 24, 2026
(shortly after the 2026 Winter Olympics).
Dovolená : 23. prosinec 2025 — 29. prosinec 2025
Holidays : December 23, 2025 — December 29, 2025
Fotosyntéza
Z Multimediaexpo.cz
Fotosyntéza (z řeckého fós, fótos – „světlo“ a synthesis – „shrnutí“, „skládání“) nebo také fotosyntetická asimilace je biochemický proces, při kterém se mění přijatá energie světelného záření na energii chemických vazeb. Využívá světelného, např. slunečního, záření a tepla k tvorbě (syntéze) energeticky bohatých organických sloučenin – cukrů – z jednoduchých anorganických látek – oxidu uhličitého (CO2) a vody. Fotosyntéza má zásadní význam pro život na Zemi. Fotosyntéza je složitý, několikastupňový proces, který probíhá v chloroplastech zelených rostlin a v mnoha dalších organismech. Jedná se o tzv. autotrofní výživu. Některé otázky týkající se jejího průběhu dosud nejsou dostatečně objasněny. Průběh se dělí do dvou fází. Ve světelné fázi barevné pigmenty pohlcují světlo, z něhož získávají energii pro následné děje. V této fázi dochází k rozkladu vody a uvolnění kyslíku, který pak využívají i jiné organismy k dýchání. Biochemické děje v temnostní fázi již světlo nepotřebují, ale využívají energii, která z něj byla ve světelné fázi získána. V této fázi dochází k zabudování oxidu uhličitého do molekul cukrů, které dále slouží buď jako zásobárna a zdroj energie, nebo jako stavební složky pro tvorbu složitějších molekul (polysacharidů, glykosidů aj.). Procesy temnostní fáze probíhají v cyklech a liší se podle druhu organismu. Vnější faktory, na nichž průběh fotosyntézy závisí, jsou světlo, teplota, voda a koncentrace oxidu uhličitého ve vzduchu. Rozlišujeme fotosyntézu oxygenní (při které vzniká kyslík a pro jejíž zahájení je potřeba voda) a anoxygenní (při které kyslík nevzniká a do jejíhož zahájení nezasahuje voda), přičemž rozeznáváme různé typy anoxygenní fotosyntézy, a to jestli je pro její zahájení potřeba sulfan nebo nějaké organické kyseliny.
Obsah |
Souhrnná rovnice oxygenní fotosyntézy
Celkový průběh fotosyntézy shrnuje rovnice:
- 6 CO2 + 12 H2O → C6H12O6 + 6 O2 + 6 H2O
Tato rovnice se však často zjednodušuje na: 6 CO2 + 6 H2O → C6H12O6 + 6 O2 Vnitřní energie získaná fotosyntézou ΔH = 2870 kJ/mol.
Historie
Na objasnění rovnice fotosyntézy se účastnila řada vědců. Tvrdým oříškem bylo také zjistit původ vznikajícího kyslíku.[1]
Rovnice
V roce 1648 vlámský lékař Jean-Baptiste van Helmont napsal, že při vypěstování vrby z výhonků v květináči se nepatrně změnila hmotnost zeminy. Ačkoliv ještě neexistoval zákon zachování hmoty, usoudil, že hmotnost rostliny se zvětšila o přijatou vodu. Dále v roce 1727 usoudil Stephen Hales, že rostliny berou část své hmoty také ze vzduchu. V roce 1771 anglický duchovní Joseph Priestley zjistil, že rostliny „napravují“ vzduch poškozený dýcháním či hořením. Později objevil kyslík, který nazval „deflogistonovaný vzduch“. Inspirován Priestleyeho pokusy roku 1779 holandský lékař Jan Ingen-Housz prokázal, že rostliny „čistí“ vzduch, pouze pokud se svítí na jejich zelené části. Švýcarský pastor Jean Senebier v roce 1782 dokázal, že se při fotosyntéze pohlcuje CO2 („svázaný vzduch“). Švýcar Nicolas-Theodoré de Saussure v roce 1804 zjistil, že hmotnost organické hmoty a kyslíku (produktů) je větší než hmotnost spotřebovaného CO2. Z toho usoudil, že se spotřebovává také voda, což byla jediná další látka, kterou do soustavy přidával. Poslední část do rovnice fotosyntézy přidal v roce 1842 německý fyziolog Robert Mayer, když došel k názoru, že fotosyntéza přeměňuje světelnou energii v energii chemickou.
Původ kyslíku
Předpokládalo se, že světlo redukuje CO2 na meziprodukt, který se slučuje s vodou na sacharid. Zdrojem kyslíku uvolněného při fotosyntéze byl podle tohoto názoru CO2. Roku 1931 Cornelius Van Niel dokázal, že zelené fotosyntetizující bakterie využívající sulfan (H2S) uvolňují síru. Vzhledem k chemické podobnosti H2O a H2S navrhl obecnou rovnici:
- CO2 + H2O + světlo → (CH2O) + O2
Tato rovnice napovídá, že fotosyntéza je dvoustupňový děj:
- Světlo se využívá k oxidaci H2{A}: 2 H2{A} + světlo → 2 {A} + 4 [H]
- Reduktans [H] pak nezávisle na světle redukuje CO2: 4 [H] + CO2 → (CH2O) + H2O
Správnost této teorie potvrdily dva pokusy:
- Roku 1937 Robert Hill zjistil, že izolované chloroplasty bez přístupu CO2, ale s umělým akceptorem elektronů (ferrikyanid [Fe(CN)6]3-), mohou tento akceptor redukovat (na ferrokyanid [Fe(CN)6]4-) a současně uvolňují kyslík. Tato tzv. Hillova reakce dokazuje, že CO2 se bezprostředně neúčastní reakce uvolňující O2. Později se zjistilo, že přirozeným akceptorem je NADP+, který se redukuje na NADPH.
- V roce 1941 Sam Ruben a Martin Kamen dokázali izotopem 18O, že zdrojem O2 je voda:
2 H218O + CO2 + světlo → (CH2O) + 18O2 + H2O
Fotosyntetizující organismy
Organismy, které zajišťují tvorbu energeticky bohatých organických látek pomocí fotosyntézy, se nazývají autotrofní, respektive fotoautotrofní. Patří mezi ně především zelené rostliny, některé druhy baktérií včetně sinic (Cyanobacteria), mnohé ruduchy (Rhodophyta), obrněnky (Dinophyta), skrytěnky (Cryptophyta), hnědé řasy (Phaeophyceae), krásnoočka (Euglenophyta) a zelené řasy (Chlorophyta). Schopnost měnit energii světla na chemickou přináší těmto organismům výhody během evoluce ve vzájemné konkurenci. Prvotní fotosyntetické systémy zřejmě byly anoxygenní, tj. neprodukovaly kyslík. Stáří nejstarších fotosyntetizujících mikroorganismů, sinic, se odhaduje na 3,5 miliardy let.[2] Kyslík v zemské atmosféře se objevil až díky oxygenní fotosyntéze. První sinice, které uvolňovaly kyslík štěpením vody, se objevily přibližně před 2 miliardami let.[3] Chloroplasty eukaryotních buněk vznikly pravděpodobně pohlcením buňky sinice, které pak žily uvnitř těchto buněk v endosymbióze a postupně se z nich staly organely. Podobným způsobem se zřejmě vyvinuly i mitochondrie u aerobních mikroorganismů. Tato teorie vzniku organel se nazývá endosymbiotická a svědčí pro ni fakt, že chloroplasty mají vlastní kruhovou DNA, stejně jako sinice.[4]
Fotosyntetický systém buňky

Fotosyntéza probíhá v chloroplastech eukaryotních buněk a v chromatoforech prokaryot. Chloroplasty jsou plastidy v cytoplazmě rostlin (především v listech) obsahujících asimilační barviva, ve kterých probíhá fotosyntéza. Mají dvojitou membránu, obsahují vlastní DNA a ribozomy. Obvykle jsou zeleně zbarveny díky chlorofylu. V základní plazmatické hmotě chloroplastů (stromatu) jsou malé, okrouhlé, na sebe navrstvené destičky (grana), která tvoří soubor uzavřených dvojitých lamel (thylakoidů) obsahujících fotosyntetická barviva (pigmenty).
- Základní pigmenty: chlorofyly a bakteriochlorofyly
- Doprovodné pigmenty: karotenoidy (karoteny a xanthofyly) a fykobiliny[5][6]
Průběh oxygenní fotosyntézy
Světelná fáze
„Světelná fáze“ či „primární děje“ jsou reakce závislé na světle a uskutečňují se v thylakoidech. Při nich probíhá přeměna světelné energie (fotonů) na chemickou energii (ve formě NADPH a ATP). Jako vedlejší produkt světelné fáze vzniká kyslík.
Absorpce fotonů
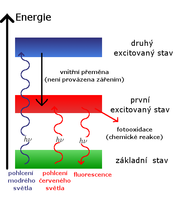
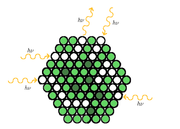
Zachycením světla rostlinným pigmentem začíná vlastní proces fotosyntézy, který spotřebuje energii světelného kvanta a přemění ji na energii chemické vazby. Vlnové délky viditelného světla mají hodnoty v intervalu 400–750 nm. Fotosyntéza zelených rostlin využívá světlo v rozsahu pouze 380–760 nm. Tomuto světlu se říká fotosynteticky aktivní záření (ve zkratce FAR nebo PhAR).[7] Různá barviva absorbují různou část světelného spektra – např. chlorofyly absorbují nejvíce světlo v modrofialové a červené části spektra. Při pohlcení červené části spektra se jako doplňková barva vyzáří zelená, odtud tedy zelená barva chloroplastů. Pokud molekula pigmentu absorbuje kvantum světelné energie, dostane se do prvního či do druhého excitovaného stavu (přeskok elektronu na vyšší energetickou hladinu). Získané energie se může molekula zbavit více způsoby, v případě fotosyntézy jsou nejdůležitější tyto čtyři:
- Vnitřní přeměnou se přebytečná excitační energie přemění na kinetickou energii pohybu molekuly, tedy na teplo. Tento děj je velmi rychlý, trvá méně než 10 ps[8]. Takto přechází chlorofyl vždy z druhého excitovaného stavu do prvního. Z toho vyplývá, že dokáže využít pouze energii odpovídající prvnímu excitovaného stavu.
- Fluorescencí je bez užitku vyzářen foton s nižší energií než přijatý. Tento pochod je pomalejší než vnitřní přeměna, trvá okolo 10 ns[8]. Takto způsobené ztráty běžně dosahují 3–6 % pohlcené energie.
- Přenos excitační energie na okolní molekuly je možný díky vzájemnému překrývání molekulových orbitalů. Velká část fotosyntetických barviv (tzv. anténní barviva) slouží pouze k absorpci fotonů a přenosu excitační energie do reakčních center, rozhodujícím akceptorem (příjemcem) je chlorofyl a. Účinnost energetického přenosu z různých doplňkových barviv na chlorofyl a se pohybuje v rozmezí 20–100 %: z karotenů 70–80 %, z fykoerythrinu a fykocyaninu 70–90 %, z chlorofylu a až 100 %.[7] Energie se z reakčního centra dále nešíří, protože je zasazen do vhodného prostředí, které snižuje energii jeho prvního excitovaného stavu a excitace je polapena.[8]
- Fotooxidace je zapříčiněna vypuzením slaběji vázaného elektronu z molekuly chlorofylu. Vzniká oxidovaná forma chlorofylu (Chl+), která má povahu kationtového volného radikálu. Vysoká energie vyexcitovaného elektronu je využita v následných chemických reakcích.
Přenos elektronů
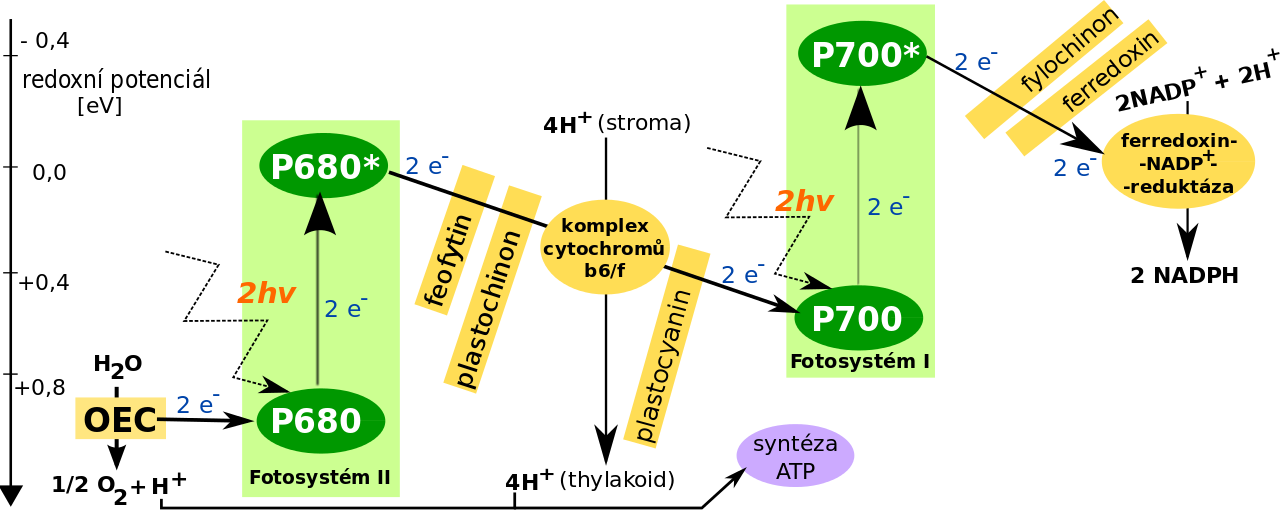
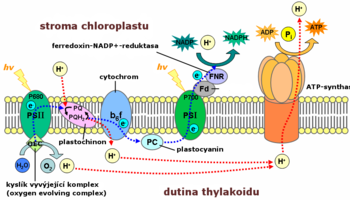
Reakce probíhají ve třech bílkovinných komplexech – fotosystému I, komplexu cytochromů b6/f a fotosystému II, které jsou propojeny pohyblivými elektronovými přenašeči. Tento přenos elektronů dostal název schéma Z, hlavní výchozí látkou je voda.
| Voda je donorem elektronů a vodíkových kationtů: | 2 H2O → O2 + 4 e- + 4 H+ | E˚' = −0,815 V[9] |
| Elektrony a vodíkové kationty se využijí k redukci: | NADP+ + H+ + 2 e- → NADPH | E˚' = −0,320 V |
| Souhrnná rovnice: | 2 NADP+ + 2 H2O → 2 NADPH + 2 H+ + O2 | E˚ = −1,135 V |
Reakce fotosystému II a fotosystému I dohromady umožňují přemístit 1 elektron a spotřebují 2 fotony. Na vznik jedné molekuly kyslíku je potřeba uvolnit a přemístit 4 elektrony (2 pro každý atom) a je tedy potřeba 8 fotonů (2 na každý elektron). Na syntézu jednoho molu glukózy je potřeba 6 × 8 = 48 molů fotonů, což odpovídá energii 8440,6 kJ/mol. Z glukózy se ale uvolní pouze 2884,5 kJ/mol, účinnost fotosyntézy je tedy 34,2 % (2884,4 × 100 % : 8440,6).[10]
Fotolýza vody
Fotosystém II (PS II) obsahuje reakční centra P680 (při vlnové délce 680 nm dosahuje absorpčního maxima – aktivace žlutozeleným světlem). V základním stavu má redoxní potenciál přes +1,0 eV,[11] ve vzbuzeném (excitovaném) okolo 0 eV. Pohlcením světla se P680 excituje na P680*. Následně je vymrštěn elektron, který velmi rychle přejde na feofytin a (Pheo a – chlorofyl a, ve kterém je Mg2+ nahrazen 2 H+) a poté zredukuje plastochinon (PQ) na plastochinol (PQH2), ze kterého přejde na komplex cytochromů b6/f. Fotosystém II vytváří silné oxidační činidlo, které je schopno oxidovat vodu, a současně slabé redukční činidlo, které redukuje slabé oxidační činidlo z fotosystému I. Fotooxidovaný P680+ (kladný náboj je důsledkem ztráty elektronu) získá elektron zpět z kyslík tvořícího komplexu (OEC – oxygen envolving complex), který získává elektrony rozkladem vody. Konkrétně oxiduje ionty OH- za vzniku peroxidu vodíku, který se rozkládá na vodu a kyslík. Komplex obsahuje vázaný mangan a každý vývoj kyslíku probíhá v 5 stavech, které se značí S0 až S4. Kroky S0 až S4 jsou oxidačně-redukční pochody poháněné energií fotonů, při přechodu ze stavu S4 na S0 se uvolní molekula kyslíku. Komplex přitom mění svoji vnitřní strukturu, pro stavy S0 až S2 je složení Mn4O4, pro stavy S3 a S4 Mn4O6. Při uvolnění molekuly O2 se komplex Mn4O6 přemění na Mn4O4. Ve tmě jsou reakční centra převážně ve stavu S1. Na vznik jedné molekuly O2 je potřeba 8 fotonů. Přitom se do dutiny thylakoidů uvolňují 4 protony z vody.
Tvorba NADPH
Fotosystém I (PS I) obsahuje reakční centra P700 (při vlnové délce 700 nm dosahuje absorpčního maxima – aktivace červeným světlem). V základním stavu má redoxní potenciál přes +0,46 eV,[11] ve vzbuzeném (excitovaném) o více než 1 eV negativnější. Pohlcením světla se P700 excituje na P700*. Následně je vymrštěn elektron, který prochází přes chlorofyl a, fylochinon (vitamín K1) a tři ferredoxiny (protein obsahující železo a síru). Díky svému velkému negativnímu redoxnímu potenciálu (−0,43 eV) je schopen v přítomnosti enzymu ferredoxin-NADP+-reduktázy redukovat NADP+ na NADPH, který je hlavním produktem tohoto tzv. necyklického přenosu, který podstupuje většina elektronů. Fotosystém I tedy vytváří slabé oxidační činidlo, které je schopno oxidovat plastocyanin, a současně silné redukční činidlo, které redukuje NADP+. Kromě necyklického přenosu je znám i cyklický přenos, při kterém se elektrony přenesou z třetího ferredoxinu na cytochrom b6/f a pomáhají tak zvyšovat přenos vodíkových kationtů (H+) ze stromatu do dutiny thylakoidu. Fotooxidovaný P700+ získá elektrony zpět přes komplex u cytochromů b6/f a plastocyanin z PS II. Energie elektronů je přitom využita k přenosu vodíkových kationtů (H+) ze stromatu do dutiny thylakoidu. Ionty H+ v dutině thylakoidu jsou využity k fotofosforylaci.
Fotofosforylace
Fotofosforylace je děj, při kterém se pomocí protonového gradientu (rozdílných koncentrací H+ mezi stromatem a thylakoidní dutinou) syntetizuje ATP. ATP vzniká z ADP a Pi (volného zbytku kyseliny fosforečné H3PO4) pomocí ATP-syntázy. Jako pohonný motor funguje vyrovnávání koncentrací protonů mezi stromatem a thylakoidní dutinou. ATP je sloučenina, která obsahuje makroergní vazby (vazby, při jejichž štěpení se uvolňuje velké množství energie). ATP i NADPH, které vznikají ve světelné fázi fotosyntézy, se využijí v temnostní fázi k tvorbě glukózy. Při vzniku jedné molekuly O2 z dvou molekul H2O se do thylakoidní dutiny uvolní 4 protony. Transportem čtyř elektronů z kyslíku se do thylakoidní dutiny pomocí cytochromu b6/f přemístí ze stromatu 8 protonů. Při redukci dvou molekul NADP+ + H+ na NADPH se vážou 4 protony ze stromatu. Celkem se tedy získá protonový gradient 12 protonů (rozdíl protonů mezi stromatem a thylakoidní dutinou). Aby byla zachována elektroneutralita, přemisťují se přes membránu ionty Mg2+ a Cl-. Při necyklickém přenosu elektronů se z 12 protonů vytvoří 4 molekuly ATP (ze 3 protonů vznikne 1 ATP) na jednu molekulu O2, což znamená, že se na jeden foton vytvoří 0,5 ATP. Kromě ATP též při necyklickém přenosu vznikají 2 molekuly NADPH a jejich energie se rovná 6 molekulám ATP (0,75 ATP na jeden foton). Celkem se tedy při necyklickém přenosu elektronů vytvoří 1,25 ATP na jeden pohlcený foton. Cyklický přenos je účinnější při přímé tvorbě ATP, protože na vznik jedné molekuly je potřeba pouze 2 protonů. Nicméně při něm nevzniká NADPH, a tak je ve výsledku výtěžek cyklické dráhy elektronu pouze 0,75 ATP na jeden pohlcený foton. (Z 12 protonů je potřeba dvou na vznik jednoho ATP. Vznikne 6 ATP na jednu molekulu O2. Po vydělení osmi získáme počet ATP vzniklých na jeden proton)[12].
Temnostní fáze
„Temnostní fáze“ či „sekundární děje“ jsou reakce nezávislé na světle. Sice neprobíhají ve tmě, ale nepotřebují světelnou energii. Temnostní reakce probíhají ve stromatu a ukládají chemickou energii získanou ve světelné fázi (ve formě NADPH a ATP) fixací CO2 do sacharidů. Jsou známy tři cykly fixace CO2 – Calvinův, Hatch-Slackův a CAM cyklus. S fotosyntézou souvisí také fotorespirační cyklus, který snižuje výnos fotosyntézy především u C3-rostlin. Různé cykly probíhají podle toho, v jakých rostlinách k nim dochází, např. C3-cyklus v pšenici, ječmeni nebo hrachu (mírný podnebný pás), C4-cyklus v kukuřici, prosu nebo cukrové třtině (subtropický podnebný pás) a CAM cyklus v kaktusech (tropický podnebný pás).
Calvinův cyklus
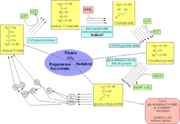
Calvinův cyklus neboli C3-cyklus (první stálé produkty, které při něm vznikají, obsahují 3 atomy uhlíku) se skládá ze 3 fází. Karboxylace neboli fixace CO2, redukce a regenerace ribulóza-1,5-bisfosfátu. Fixace CO2 na ribulóza-1,5-bisfosfát je katalyzována enzymem RuBisCO (ribulóza-1,5-bisfosfát-karboxyláza/oxygenáza). Vzniklý adiční produkt se štěpí na 2 molekuly 3-fosfoglycerátu. Ten se pomocí enzymu a NADPH redukuje na glyceraldehyd-3-fosfát. Vždy jedna molekula glyceraldehyd-3-fosfátu ze 6 opouští cyklus a syntetizují se z ní další látky (sacharidy, škrob, bílkoviny atd.). Ze zbývajících pěti molekul glyceraldehyd-3-fosfátu v regenerační fázi vznikají opět 3 molekuly ribulóza-5-fosfátu a jejich následnou fosforylací ATP vznikají 3 molekuly ribulóza-1,5-bisfosfátu. Calvinův cyklus se tak uzavírá. Ze tří molekul ribulóza-1,5-bisfosfátu a tří molekul CO2, vzniknou tři molekuly ribulóza-1,5-bisfosfátu a jedna molekula glyceraldehyd-3-fosfátu. C3-cyklus využívají především rostliny mírného a chladných pásů, protože teplota v těchto oblastech není vysoká a fotorespirace nepřevládá nad fotosyntézou.
Hatch-Slackův cyklus
Rostliny, v nichž probíhá Hatch-Slackův cyklus neboli C4-cyklus (vznikají látky se 4 atomy uhlíku), se vyznačují charakteristickou anatomickou stavbou. Obsahují mezofylové buňky (fixace CO2) a buňky pochvy cévního svazku (uvolnění CO2 do Calvinova cyklu). V chloroplastech mezofylových buněk chybí enzym RuBisCO a CO2 se váže tak, že HCO3- reaguje s fosfoenolpyruátem za vzniku oxalacetátu. Oxalacetát je za pomoci enzymu malátdehydrogenázy a NADPH redukován na malát. Malát přechází do buněk pochvy cévního svazku, kde je pomocí NADP+ oxidován na pyruát a současně se uvolní CO2. Ten pokračuje do Calvinova cyklu. Pyruvát se vrací do buněk mezofylu, kde je za spotřeby ATP fosforylován na fosfoenolpyruát. C4 cyklus využívají především teplomilné rostliny, protože při zvýšené teplotě se více uplatňuje fotorespirace, a tím klesá účinnost fotosyntézy, proto koncentrují CO2 před tím, než vejde do Calvinova cyklu.
CAM cyklus
CAM cyklus neboli Crassulacean Acid Metabolism (metabolismus kyselin u tučnolistých rostlin, u kterých byl tento cyklus poprvé pozorován), je obměnou Hatch-Slackova cyklu. CO2 je v noci ukládán jako zásoba do vakuol a ve dne opětovně zpracován Calvinovým cyklem.
Tento cyklus využívají pouštní rostliny (např. sukulenty), které musí velmi šetřit vodou, a proto otevírají průduchy jenom v noci, kdy vážou CO2 do malátu. Pro uložení zásoby CO2 potřebují velké množství fosfoenolpyruátu, který získávají glykolytickým štěpením škrobu. Během dne se malát štěpí na CO2, který vstupuje do Calvinova cyklu, a na pyruát, ze kterého se opět syntetizuje škrob. Takto provádějí CAM rostliny fotosyntézu s minimálními ztrátami vody.
Fotorespirace
Fotorespirace neboli světelné dýchání rostlin je ve své podstatě proces opačný k fotosyntéze. Rostlina při něm přijímá kyslík a produkuje CO2. Při fotorespiraci se ovšem neuvolňuje ATP (energie), ale dochází ke štěpení meziproduktů fotosyntézy, produkci oxidu uhličitého, a tím ke ztrátám na substrátu a energii. Fotorespirace je způsobena karboxylačně-oxidační aktivitou enzymu RuBisCO (ribulóza-1,5-bisfosfátkarboxyláza/oxygenáza). Za běžných atmosférických podmínek při 25 °C převažuje karboxylace nad oxygenací v poměru asi 4:1. Fotorespirace je významná hlavně u C3-rostlin.
Při fotorespiraci vznikne navázáním kyslíku na ribulóza-1,5-bisfosfát pětiuhlíkatý meziprodukt, který není stálý a rozpadá se na 3-fosfoglycerát a 2-fosfoglykolát. 3-fosfoglycerát vstoupí do Calvinova cyklu, zatímco 2-fosfoglykolát je dále metabolizován a může být využit k syntéze některých látek (aminokyselin). Většina je však rozložena až na CO2. Fotorespirace neprobíhá pouze ve chloroplastech, ale jednotlivé fáze se uskutečňují také v cytosolu, peroxisomech a mitochondriích.
Rychlost fotosyntézy
Nejčastěji se stanovuje z měření produkce O2 nebo spotřeby CO2. Závisí na řadě faktorů, vnitřních i vnějších, které nepůsobí samy o sobě, ale vzájemně podmíněně. Z vnitřních faktorů jde zejména o množství chlorofylu, stáří listů a minerální výživu. Mezi vnější činitele patří:
- Světlo – fotosyntézu ovlivňuje spektrálním složením, které se mění s výškou Slunce a intenzitou záření. Rostoucí intenzita může rychlost zvyšovat jen do určité úrovně.
- Koncentrace CO2 – v ovzduší asi 0,03 % (není optimální, rostliny potřebují více), závislost rychlosti fotosyntézy na množství CO2 je přibližně stejného charakteru jako u světla. Lze zvýšit přesunutím rostlin do skleníku.
- Teplota – výrazně ovlivňuje fotosyntézu, u našich rostlin je optimum asi 15–25 °C, při teplotách nad 30 °C nastává výrazný pokles rychlosti.
- Voda – je zcela nezbytná, nedostatek se projevuje uzavíráním průduchů, což způsobí zastavení přístupu CO2.
Světlo
Fotosyntézu ovlivňuje spektrum a intenzita světelného záření.
Spektrum vhodné pro fotosyntézu (FAR) je v rozmezí 380–760 nm. Přechodem od červených k fialovým paprskům se kvantový zisk snižuje, i když se snižující se absorpce chlorofylů částečně kompenzuje doprovodnými pigmenty. Jejich efektivnost je však menší než u chlorofylů. Minimální intenzita světla pro začátek fotosyntézy je u různých rostlin různá. Některým stačí již intenzita petrolejové lampy, řasy (Algae) fotosyntetizují v hloubce vody, kde má záření intenzitu měsíčního světla.[13] S přibývající intenzitou světla se rychlost fotosyntézy zvyšuje. V okamžiku, kdy se příjem a výdej CO2 vyrovná, nastává tzv. kompenzační světelný bod. Rychlost fotosyntézy pak dále roste až do bodu světelného nasycení, kdy se ustálí. Při vysokých intenzitách světla vzniká velké množství kyslíkových radikálů, které by mohly porušit fotosystém II, a tak zastavit fotosyntézu. Rostliny proto obětují bílkovinu D1 (OEC – bílkovinný komplex s manganem, který vyvíjí kyslík), aby zamezily vzniku nebezpečných radikálů. Tuto bílkovinu mohou rostliny při zlepšení podmínek velmi rychle opět nasyntetizovat, protože gen pro její vznik je uložen v DNA chloroplastu. Rostliny se proti vysoké intenzitě světla brání tím, že na čas přeruší svůj fotosyntetický aparát. Závislost intenzity světla znázorňuje světelná křivka fotosyntézy. Rostliny se podle požadavků dělí na světlomilné a stínomilné.
- Stínomilné (sciofyty) vyžadují nižší intenzitu světla. Obsahují více zelených a žlutých pigmentů (chlorofyly, xanthofyly), intenzivněji využívají modrofialové světlo. Odpovídá jim uvedená světelná křivka.
- Světlomilné (heliofyty) mají vysoké požadavky na intenzitu světla. Obsahují méně karotenoidů a intenzivněji využívají červené světlo. Jejich světelná křivka fotosyntézy má menší úhel a delší podíl „lineární části“. Kompenzační bod a bod světelného nasycení leží při vyšších intenzitách záření.
Koncentrace CO2
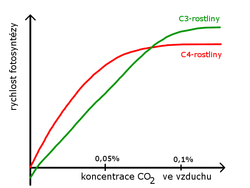
Vzdušný oxid uhličitý je hlavním dodavatelem CO2 pro fotosyntézu. Jeho koncentrace ve vzduchu kolísá od 0,02–0,03 %. Nejnižší koncentrace, při níž začíná fotosyntéza, je 0,008–0,010 %. Při zvyšování koncentrace se rychlost fotosyntézy zvyšuje. Místo, kde je příjem a výdej CO2 vyrovnán, se nazývá kompenzační bod. Fotosyntéza se dále zvyšuje až do nasycení, kdy se ustálí (0,06–0,4 %). Zvyšováním za hranici 2–5 % CO2 ve vzduchu fotosyntéza ustane.[14] Graf čisté fotosyntézy v závislosti na koncentraci CO2 začíná u C3-rostlin v záporných hodnotách. Důvodem je výrazná fotorespirace. C4-rostliny mají mechanismus zajišťující koncentrování CO2 (Hatch-Slackův cyklus) a fotorespirace je u nich téměř potlačena. Proto také dosáhnou bodu nasycení dříve.
Teplota
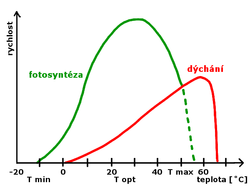
Průběh reakcí obecně urychluje zvýšení teploty o 10 °C 2–3krát.[15] Rychlost fotosyntézy závisí na teplotě exponenciálně a limitujícím faktorem je intenzita světla. Jelikož teplota ovlivňuje i další fyziologické pochody, je závislost fotosyntézy na ní složitá. Při nízkých teplotách rostliny fotosyntetizují pomalu. Zvyšováním teploty rychlost roste až po hranici teplotního optima. Poté pomalu klesá a při 35–45 °C se zastavuje. Současně s fotosyntézou se však zvyšuje i dýchání a obě rychlosti se zvyšují nerovnoměrně.[15] Vliv teploty na fotosyntézu se výrazněji projevuje při vyšší intenzitě světla. Různý vliv má teplota u C3 a C4-rostlin. Evolucí rostlin došlo k adaptaci na různé teplotní podmínky.[15]
| Rostlina | Minimum |
|---|---|
| Jehličnany | -15 až -5 °C |
| Ozimá pšenice | -5 až 0 °C |
| Teplomilné rostliny | 3 až 5 °C |
| Rostliny mírného pásu | okolo 0 °C |
| Subtropické rostliny | 0 až 2 °C |
| Vodní tropické rostliny | 4 až 8 °C |
| Rostliny | Optimum |
| mírného pásu | 25 až 30 °C |
| přízemní | 8 až 15 °C |
| vodní teplomilné | 40 °C |
| Rostliny | Maximum |
| některé vysokohorské | 12 °C |
| teplomilné | 50 °C (až 80 °C) |
Voda
Působnost vody je přímá i nepřímá, a proto je závislost fotosyntézy na vodě složitá. Voda
- působí jako donor vodíku,
- hydratuje asimilační pletiva,
- ovládá regulaci velikosti štěrbiny průduchů a transpiraci,
- ovlivňuje růst asimilační plochy,
- přivádí ionty prvků,
- rozvádí asimiláty.
Maximální rychlost fotosyntézy je při vodním deficitu 5–25 % plného nasycení vodou. V rozmezí deficitu 40–60 % se rychlost výrazně snižuje a klesá k nule. Snížení množství vody vede k zavírání průduchů, a tím k menšímu příjmu CO2.[16] Nedostatek vody ovlivňuje i složení produktů fotosyntézy. Převládají spíše jednoduché látky (např. osmoticky aktivní látky jako sacharidy a aminokyseliny) a tvorba makromolekulárních látek (bílkovin) je snížena.
Anoxygenní fotosyntéza
Nižší fotosyntetizující mikroorganismy (např. sirné bakterie) používají jako donory vodíku místo vody sirovodík (H2S) nebo organické kyseliny. Nedochází při tom k uvolňování kyslíku. Proces se proto označuje jako anoxygenní fotosyntéza. Tento proces je však oproti oxygenní fotosyntéze mnohem méně efektivní z hlediska využití energie, ΔH = 357 kJ/mol (hodnota vztažená na fixaci 1 molu CO2; v případě oxygenní fotosyntézy 475 kJ/mol). Souhrnná rovnice anoxygenní fotosyntézy využívající sirovodík je:[17] CO2 + 2 H2S → (CH2O) + 2 S + H2O Obecnou rovnici anoxygenní fotosyntézy viz v části Původ kyslíku.
Význam fotosyntézy
Fotosyntéza je z hlediska existence současného života pokládána za jeden z nejdůležitějších biochemických procesů (podle některých autorů přímo nejdůležitější[18]). Bez ní by biosféra v současné podobě nebyla zásobena organickými látkami nebo jen ve velmi omezené míře (chemoautotrofními bakteriemi). Organické látky vytvářené při fotosyntéze spotřebovávají heterotrofní organismy, mezi které patří i člověk, při své výživě.[19] Fototrofní organismy ročně zachytí asi 1071 kJ energie a její pomocí vyrobí asi 14×1011 t organické hmoty, uvolní 15×1011 t O2 a fixují 20×1011 t CO2 ze vzduchu a oceánů.[20] Na produktech fotosyntézy je závislý i dnešní průmysl, neboť uhlí, ropa a zemní plyn (tzv. fosilní paliva) jsou zbytky organismů, které žily v dávné minulosti a bez fotosyntézy by nevznikly.[19] Procesem s opačným průběhem než oxygenní fotosyntéza je buněčné dýchání (respirace), kdy se fotosyntézou a následnými procesy energie nahromaděná do chemických látek uvolňuje oxidací za spotřeby vzdušného kyslíku (O2) a přeměňuje se na adenosintrifosfát (ATP). Jako ATP je tato energie přímo dostupná pro další potřebné reakce v těle organismu.
Literatura
- KARLSON, P. Základy biochemie. Praha : Academia, 1981.
- ŠEBÁNEK, J., et al Fyziologie rostlin. 1. vyd. Praha : Státní zemědělské nakladatelství, 1983.
- VODRÁŽKA, Z. Biochemie 3. Praha : Academia, 1993. ISBN 80-200-0471-8. S. 55–65.
- VOET, D.; VOETOVÁ, J. Biochemie. 1. čes. vyd. Praha : Victoria Publishing, 1995. ISBN 80-85605-44-9.
Reference
- ↑ VOET, D.; VOETOVÁ, J. Biochemie. 1. čes. vyd. Praha : Victoria Publishing, 1995. ISBN 80-85605-44-9. S. 657–658, 659–660.
- ↑ AWRAMIK, S. M.. The oldest records of photosynthesis. Photosynthesis Research, 1992, roč. 33, s. 75–89. Dostupné online. ISSN 1573-5079.
- ↑ RIVAS, J. L.; BALSERA, M.; BARBER, J.. Evolution of oxygenic photosynthesis: genome-wide analysis of the OEC extrinsic proteins. Trends in Plant Science, 1992, roč. 9, čís. 1, s. 18–25. Dostupné online. ISSN 1360-1385.
- ↑ KIMBALL, J. W.. Endosymbiosis and The Origin of Eukaryotes [online]. [Andover, Massachusetts?] : John W. Kimball, 2007-08-22, [cit. 2008-01-30]. Dostupné online. (anglicky)
- ↑ VOET, D.; VOETOVÁ, J. Biochemie. 1. čes. vyd. Praha : Victoria Publishing, 1995. ISBN 80-85605-44-9. S. 664.
- ↑ ŠEBÁNEK, J., et al Fyziologie rostlin. 1. vyd. Praha : Státní zemědělské nakladatelství, 1983. S. 145–146.
- ↑ 7,0 7,1 ŠEBÁNEK, J., et al Fyziologie rostlin. 1. vyd. Praha : Státní zemědělské nakladatelství, 1983. S. 151–152.
- ↑ 8,0 8,1 8,2 VOET, D.; VOETOVÁ, J. Biochemie. 1. čes. vyd. Praha : Victoria Publishing, 1995. ISBN 80-85605-44-9. S. 661–663.
- ↑ VOET, D.; VOETOVÁ, J. Biochemie. 1. čes. vyd. Praha : Victoria Publishing, 1995. ISBN 80-85605-44-9. S. 670.
- ↑ ŠEBÁNEK, J., et al Fyziologie rostlin. 1. vyd. Praha : Státní zemědělské nakladatelství, 1983. S. 151.
- ↑ 11,0 11,1 KARLSON, P. Základy biochemie. Praha : Academia, 1981. S. 325–326.
- ↑ VOET, D.; VOETOVÁ, J. Biochemie. 1. čes. vyd. Praha : Victoria Publishing, 1995. ISBN 80-85605-44-9. S. 679–679.
- ↑ ŠEBÁNEK, J., et al Fyziologie rostlin. 1. vyd. Praha : Státní zemědělské nakladatelství, 1983. S. 161.
- ↑ ŠEBÁNEK, J., et al Fyziologie rostlin. 1. vyd. Praha : Státní zemědělské nakladatelství, 1983. S. 163–165.
- ↑ 15,0 15,1 15,2 ŠEBÁNEK, J., et al Fyziologie rostlin. 1. vyd. Praha : Státní zemědělské nakladatelství, 1983. S. 166–168.
- ↑ ŠEBÁNEK, J., et al Fyziologie rostlin. 1. vyd. Praha : Státní zemědělské nakladatelství, 1983. S. 169.
- ↑ VODRÁŽKA, Z. Biochemie 3. Praha : Academia, 1993. ISBN 80-200-0471-8. S. 56, 65.
- ↑ KARLSON, P. Základy biochemie. Praha : Academia, 1981. S. 323.
- ↑ 19,0 19,1 KARLSON, P. Základy biochemie. Praha : Academia, 1965. S. 303.
- ↑ VODRÁŽKA, Z. Biochemie 3. Praha : Academia, 1993. ISBN 80-200-0471-8. S. 55.
Externí odkazy
- BECK, E. G. Photosynthese (Biologiekurs Klasse 12) [online]. StD Ernst-Georg Beck, [1997-10-01?], rev. 2005-02-?, [cit. 2007-12-12]. Dostupné online. (německy)
- HELMICH, U. Photosynthese [online]. 2006-12-?, [cit. 2007-12-12]. Dostupné online. (německy)
- PREUSS, A. Photosynthese – Pflanzen verwerten Lichtenergie [online]. Münster : Westfälische Wilhelms-Universität, 1997-01-12, rev. 1997-09-23, [cit. 2007-12-12]. Dostupné online. (německy)
- SENGBUSCH, P. Photosynthese. Hamburg : Universität Hamburg, Department Biologie, rev. 2003-07-31, (Botanik online, cit. 2007-12-12, německy)
- Ideje.cz – Realizace fotosyntézy v laboratoři (cit. 2008-8-21)
- (anglicky) Photosynthesis (Virtual Cell) - video na Youtube
|
| Náklady na energie a provoz naší encyklopedie prudce vzrostly. Potřebujeme vaši podporu... Kolik ?? To je na Vás. Náš FIO účet — 2500575897 / 2010 |
|---|
| Informace o článku.
Článek je převzat z Wikipedie, otevřené encyklopedie, do které přispívají dobrovolníci z celého světa. |